Calloselasma rhodostoma
Malayen-Mokassinotter (Kuhl, 1824)
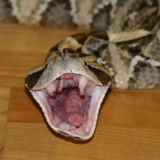
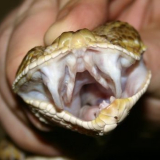
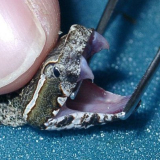
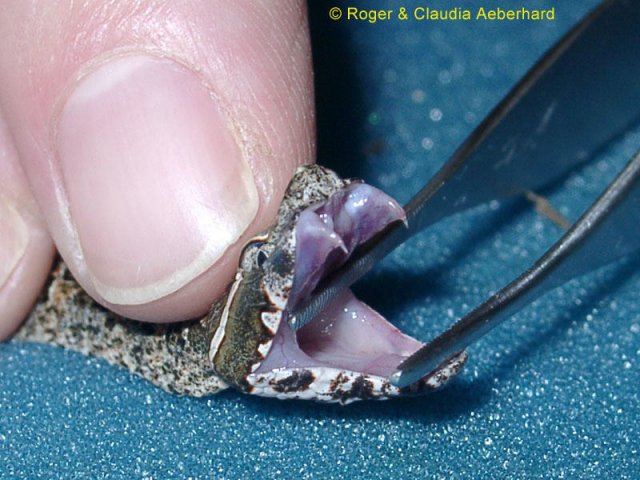
Der lanzenförmig dreieckige Kopf setzt sich deutlich vom Hals ab. Die Grundfärbung der Oberseite ist rotbraun mit winkligen dunkelbraunen bis schwarzen Flecken. Auf der Rückenmitte verläuft eine dunkle Längslinie. Die gelblich-weisse Bauchseite ist dunkel punktiert. Die Männchen sind nicht nur kleiner als die Weibchen, sie haben auch meist viel Rot in der Musterung wo hingegen die Weibchen mehr im braunton sind, eventuell wegen der Tarnung für das Ausbrüten der Eier. Weiter besitzen sie 2 Prä- und 2 Postocularia sowie ein Lorealschild. 7 bis 8 Oberlippenschilde und 11 bis 12 Unterlippenschilde. Die Reihe der ungekielten Schuppen beträgt 21 in der Körpermitte.
Länge: 80 - 100 cm
Lebensraum
Das Verbreitungsgebiet erstreckt sich über Thailand, Kambodscha, Laos, Vietnam, die Malayischen Halbinseln, Sumatra und Java.
Diese Grubenotter bevorzugt ein Klima mit ausgeprägten Regen- und Trockenzeiten. In den Monaten Juli und August, Regenzeit, sollte man jeden Tag das Terrarium und die Tiere mit Handwarmem Wasser besprühen. Sie lebt in lichten Waldungen, in Gummiplantagen und an Feldrändern. Sie ist dämmerungsaktiv und beisst bei der geringsten Störung sofort zu. Sie ist äusserst Aufmerksam und beobachtet einem immer. Wenn man mit Futter kommt so reagiert sie sofort.
Sie ernährt sich von Eidechsen, Fröschen und Mäusen. Vor allem die Jungtiere fressen in den ersten Monaten vor allem Kaulquappen. Hat man keine, muss man leider fast immer die Jungtiere stopfen.
Sie legt im August oder September ( bei mir auch schon anfangs Juni ) bis über 40 Eier, die ich in Erde lege und bei 28° C und 70 bis 80% Luftfeuchtigkeit ausbrühte. Die Jungtiere schlüpfen nach 35–50 Tagen. In der Wildnis macht das Weibchen eine Brutpflege indem sie sich über die Eier legt und diese bei Gefahr verteidigt.
Haltung und Zucht
Es reicht ein mittelgrosses Terrarium. Es soll 10–12 Stunden beleuchtet werden und weitgehend konstante Luft- und Bodentemperaturen zwischen 26 – 28° C aufweisen. Am besten erstellt man mittels Korkrinden eine erhöhte Plattform unter der Beleuchtung oder einem Spot, wo sie bei Temperaturen bis 32° C Wärme tanken kann, bei bedarf. Als Bodengrund verwendet man ein Gemisch aus feinem Sand und Walderde. Ein grösseres flaches Wasserbecken und einige Korkrinden als Unterschlupf sollten nicht fehlen. Aufgepasst: Die Calloselasma bringt es fertig, in einem Wasserbecken dass zu tief ist, zu ertrinken.
Das Gift führt zu starken Ödemen und zu massiven Störungen im Mechanismus der Blutgerinnung. Aus diesem Grunde wird das Gift von ihr, in der Medizin in zunehmendem Masse zum Auflösen von Blutgerinnseln innerhalb der Blutbahn verwendet.
Der Umgang mit dem Haken ist nicht immer einfach. Manchmal, jedoch eher selten bleiben sie schön auf einem Haken. Mit zwei Haken hat man schon viel mehr Erfolg sie von A nach B zu bringen. Beim Fixieren ist es sehr Wichtig auch gleich den Körper zumindest nach dem ersten drittel zu Halten. Sie drehen sich gerne ein paar mal um die eigene Achse bis man sie entweder erwürgt oder losläst.
Nachzuchtbeispiele:
Am 04.09.2005 hat ein Weibchen 32 Eier gelegt. Da wir schon viele andere Nachzuchten hatten wollten wir nicht alle Ausbrüten. Zwischen dem 12. und 15.10.2006, also nach 38 und 41 Tage sind 8 Junge geschlüpft. Sie hatten ein Gewicht von 3,1 bis 4,4 gramm und Längen zwischen 15 und 18 cm.
Am 09.08.2006 hat uns ein anderes Weibchen über 30 Eier gelegt. Da die Calloselasma rhodostoma eine Brutpflege betreibt haben wir ihr die Eier gelassen. Obwohl wir immer wieder rund ums Gelege Wasser gespritzt haben um die Luftfeuchtigkeit hoch zu halten sind nur 4 Junge geschlüpft die mit 3,2g durchschnittlich knapp 1 ½ g leichter waren als die Jungen die Ausgebrütet wurden.
Am 12. und 13.08.06 hatte und das andere Weibchen 45 Eier Gelegt. Dieses mal haben wir alle Eier Inkubiert.
Zwischen dem 22.9 und 24.09.06 sind 41 Junge geschlüpft. Sie waren 4,6 bis 6,1 gramm schwer und 18 bis 21 cm lang.
Am 26.08.07 hat uns ein Weibchen ca. 22 Eier gelegt. Am 11.10.07, also nach 46 Tagen sind die Jungen allesamt geschlüpft, wie auf Komando. Interessanterweise haben die ersten 2 Tiere schon von Anfang an selbständig nackte Mäuse gefressen. Weitere 4 Tiere nach dem ersten mal Stopfen.
Aufzucht
Da die Calloselasma rhodostoma in der Natur sich in der ersten Zeit von kleinen Fröschen, Qaulquappen, Würmer, Insekten und sonstigem ernährt, und erst später auch Nagetiere frisst, so bleibt einem oft nichts anderes Übrig, als die kleinen 2 bis 4 Monate lang zu stopfen. Auch die Grösse der Babys ist ein Problem. Selten habe ich so kleine frischgeborene Mäuse zum verfüttern. Aus diesem Grund stopfe ich die kleinen die erste Zeit mit Rinderherz-Streifen, bis sie etwas grösser sind und dann eventuell kleine Mäuse nehmen. Auch hier erfolgt die Aufzucht einzeln in kleinen Boxen. Etwas Erde, ein Rindenstück und ein kleines Wasserbecken reichen. Einfach wieder einmal bei ein paar Jungen eine frischgeborene wirklich kleine Maus über Nacht in die Box und hoffen dass sie frisst. Manchmal gibt es Exemplare die auch schon nach einem Monat selbständig Mäuse fressen.
Giftwirkung und Symptome, die bei einem Vollbiss eintreten können:
Autopharmakologische Gifteffekte
Gastrointestinale, pulmonale und kutane Symptome und Befunde, die auf autopharmakologischen Prozessen beruhen könnten, sind selten oder wurden überhaupt nicht beobachtet.
Lokale Gifteffekte
- Lokale Schmerzen korreliert mit dem Schweregrad der Vergiftung.
- Lokale Schwellung beginnt Minuten nach dem Biss und kann bis über 12 Std. dauern, bis das maximale Ausmass erreicht ist. Eventuell Hypovolämischer Schock.
- Extravasation, Blasenbildung (Hämorrhaginwirkung) und systemische Vergiftung. Extravasation von Erythrozyten und Plasma führt zu einer Verfärbung der Haut.
- Lokale Nekrosen
Hämotoxische Gifteffekte
- Systemische Blutung tritt bei schwerer systemischer Vergiftung auf.
- Hämoptysis bei Patienten mit Lungenkavernen (Tuberkulose).
- Diskoide Ekchymosen, Gingivablutung, Persistierende Sickerblutung, Hämatemesis, Intrazerebrale Blutung.
- Hypovolämie (Flüssigkeits- und Erythrozytenverlust in dem Bereich der Schwellung) – Schock
Morbidität
- Der lokale nekrotisierende Effekt des Giftes ist eine häufige Morbiditätsursache. Gangrän führt zum Verlust von Zehen, Fingern oder ganzen Extremitäten.
- Lokale Nekrosen vor allem bei Bissen an Fingern und Zehen und wenn Tourniquets verwendet wurde.
- Die Ungerinnbarkeit des Blutes scheint nicht mit einem hohen Risiko von systemischen Blutungen, ausgenommen Blutverluste in die lokale Schwellung, verbunden zu sein.
Therapie
- Bluttransfusion: Verbesserung bei Patienten mit Schock oder mit einer Anämie, kein Effekt auf die Dauer des Gerinnungsdefekts.
- Fibrinogen: Verbesserung einiger Hämostaseparameter, kein bleibender Effekt.
- Prophylaktische Antiinfektion und Tetanusprophylaxe.
Antivenin
- Monovalent, Malayan pit viper antivenin
Wirksamkeit des Antivenin
- Keine Wirksamkeit bezüglich lokaler Schwellung.
- Keine Wirksamkeit auf die Entwicklung von Nekrosen, wenn mehr als eine Stunde nach dem Biss vergangen ist.
- Wirksam bezüglich der Schocksymptomatik.
Hämostaseeffekt:
Klinisch; Gingivablutungen sistieren innerhalb einer Stunde und sollten nicht wieder auftreten.
Koagulationsdefekt:
Bei intravenöser Verabreichung normalisiert sich die Gerinnungsfähigkeit des Blutes innerhalb von 1 bis 18 Std. Wird zu wenig Antivenin verabreicht, wird keine komplette Wiederherstellung erreicht, und es tritt nach 20 bis 130 Std. erneut die Ungerinnbarkeit des Blutes ein.
Es sollten 60 bis 100 ml Antivenin verabreicht werden.
Achtung: Anaphylaktische Reaktionen sehr wahrscheinlich.
Erste Hilfe
- Notarzt- Ambulanz anrufen und Ruhe bewahren.
- Eventuell mit Saugglocke versuchen Gift abzusaugen.
- Keine Kompressionsbinde anlegen.
- Schneiden ist Sache des Arztes.