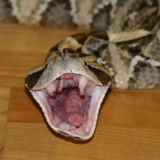
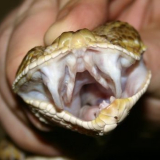
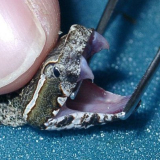
Enzyme haben sich phylogenetisch aus Verdauungsenzymen entwickelt, und sind in Schlangengiften reichlich vorhanden.
Sie lassen sich in folgende Gruppen einteilen:
1. Hyaluronidasen sind als nichttoxische Hilfsstoffe in zahlreichen Giften vorhanden. Durch Spaltung der hochviskösen Hyaluronsäure des Bindegewebes erleichtern sie die Ausbreitung aller Komponenten. Sie werden daher als Spreadingfaktoren bezeichnet.
2. Phospholipasen sind sämtlich vom Typ A2, katalysieren also einen einfachen hydrolytischen Prozess. Sie sind wie Hyaluronidasen in allen Schlangengiften vorhanden. Zellschädigungen durch Phospholipasen werden hervorgerufen, wenn sie von Enzymen aufgeschlossen werden. Einige Phospholipasen werden durch Peptide in ihrer pharmakologischen Wirksamkeit verstärkt. Zum Beispiel den Crotoxinkomplex, der aus dem sauren Crotapotin und dem basischen Enzym besteht. Der Komplex löst sich erst, wenn das Enzym auf sein Substrat trifft, wo es seine volle Toxizität entfaltet. Es gibt auch Phospholipasen die aus Komplexen zwischen verwandten Einzelbestandteilen bestehen. Z. B. Taipoxin.
Manche Enzyme dieser Gruppe richten sich meist selektiv gegen bestimmte membranale Strukturen, wie Notexin oder Bungarotoxin. Auch die Crotoxinphospholipase weißt einen Bezug zu einem besonderen Substrat auf. Die genannten Enzyme sind einerseits besonders neurotrop, und bevorzugt die Transmitterfreisetzung durch präsynaptischen Angriff blockieren. Dadurch ergänzen sie die rein postsynaptisch wirkenden Peptiden.
Auch die myotoxischen Wirkungen beruhen im wesentlichen auf Phospholipasen A.
3. Die Proteasen, genauso vielfältig in ihrer unterschiedlichen Spezifität, hat erhebliche toxikologische Konsequenzen. Abgesehen von einigen neurotoxischen Phospholipasen bestimmen die Proteasen das Vergiftungsbild nach Vipernbissen.
Einige Proteasen greifen bevorzugt solche Substrate an, denen eine besondere biologische Bedeutung zukommt. Zum Beispiel die Hämorrhagine, die gerinnungwirksamen Proteasen und die P. mit Kallikrein, - bzw. Kininaseaktivität.
Hämorrhagine sind in vielen Vipern und Crotaliden – Giften vorhanden, und bestimmen nicht selten das Vergiftungsbild. Sie hydrolysieren den vor allem aus Kollagen bestehenden Halteapparat der kleinsten Gefässe. Die geschwächte Basalmembran wird überdehnt und reisst. Erythrozyten treten in das umgehende Bindegewebe aus. Im Gegensatz zu den Hämorrhaginen führt die überaus heterogene Gruppe der Permeabilitätsfaktoren zur Ausbildung interendothelialer Spalten, ohne den Halteapparat zu beeinflussen.
Gerinnungswirksame Proteasen können die Gerinnung auf verschiedene Arten aktivieren oder hemmen. Echis carinatus – Gift setzt Thrombin aus Prothrombin frei, Calloselasma rhodostoma und Bothrops jararaca– Gift wirkt thrombinähnlich auf Fibrinogen.
Die Hyperkoagulabilität, vor allem nach Vipergiften, führt in der Regel zu einer Verbrauchskoagulopathie mit entsprechender Blutungsneigung. Sie wird durch die Gewebsschädigung um die Bissstelle noch verstärkt sowie auch durch die lokale und systemische Wirkung der Hämorrhagine. Zu beachten ist auch die Wirkung von Proteasen auf das Kininsystem. Einige Endopeptidasen können das Nonapeptid Bradykinin aus seinen Vorstufen, den Kininogenen des Blutplasmas freilegen, Kininasen verkürzen das Peptid um sein C- terminales Arginin oder zerlegen es in grössere Fragmente. Ein Kininasehemmstoff, Bradykinin potentiating factor genannt, erhöht die venoläre Permeabilität für Proteine, erzeugt Schmerz und senkt den arteriellen Druck. Neben Bradykinin gibt es jedoch noch andere, thermolabile Giftkomponenten, die den arteriellen Druck langsam und langanhaltend senken und wohl pathogenetisch wichtig sind.